Лаборатория осуществляет свою деятельность в форме административных процедур в отношении юридических лиц всех форм собственности и индивидуальных предпринимателей, осуществляющих коммерческую деятельность на фармацевтическом рынке Республики Беларусь, на основе двусторонних договоров на хозрасчетной основе.
Основные направления деятельности лаборатории:
посерийная проверка качества биологических лекарственных средств до поступления их в реализацию на территории Республики Беларусь;
контроль качества лекарственных средств, находящихся в обращении на территории Республики Беларусь
испытание лекарственных средств на стадии их регистрации на территории страны;
испытания и исследования лекарственных средств, ветеринарных препаратов, выполняемые по заявкам сторонних предприятий и организаций, экспертиза методик и программ испытаний и исследований, в пределах областей аккредитации, технических возможностей испытательного оборудования и компетентности персонала;
адаптация и апробация новых методик исследования качества ИЛС;
совершенствование методов контроля качества ИЛС;
экспертиза ТНПА;
Лаборатория проводит проверку качества ИЛС на соответствие требований нормативного документа производителя. Лаборатория гарантирует неукоснительное соблюдение национальных интересов и приоритетов в области охраны здоровья населения, развитии контроля качества и производства иммунобиологических лекарственных средств.

В соответствии с приказом Министерства здравоохранения Республики Беларусь от 18.03.2009 № 287 «О совершенствовании контроля за качеством иммунобиологических лекарственных средств и работы по коллекционированию вирусов и бактерий, патогенных для человека» в Республиканском научно-практическом центре эпидемиологии и микробиологии 13.08.2010 была создана лаборатория контроля качества иммунобиологических лекарственных средств (далее – лаборатория). Создание независимой лаборатории по контролю качества ИЛС обосновано действующими международными требованиями, в соответствии с которыми каждое государство, даже не производящее вакцины, должно иметь национальный орган контроля иммунобиологических препаратов.
Лаборатория создана с целью проведения государственной политики обеспечения качества и предотвращения поступления на внутренний рынок республики некачественных иммунобиологических лекарственных средств (далее – ИЛС). Лаборатория аккредитована в Системе аккредитации Республики Беларусь на соответствие требованиям ГОСТ ISO/IEC 17025-2019 (Аттестат № BY/112 1.1222 от 22.01.1996).
В 2017-2018 гг. лаборатория участвовала в международном проекте по программе «Международная аккредитация лабораторий для испытания продукции медицинского назначения и поддержка здравоохранения в Беларуси (BELMED)» (номер CRIS: ENPI/2013/024-679). В результате реализации проекта лаборатория была оснащена современным оборудованием, позволяющим проводить широкий спектр испытаний, сотрудники лаборатории прошли обучение по актуальным направлениям лабораторной деятельности.

Вероника Петровна ШИМАНОВИЧ
Заведующая лабораторией
кандидат медицинских наук
Тел.: +375-17 272 04 15
E-mail: lqcim@belriem.by
В настоящее время в лаборатории работают 10 сотрудников, в том числе один кандидат медицинских наук, один кандидат биологических наук, доцент:
Шиманович Вероника Петровна – заведующий лабораторией, кандидат медицинских наук;
Капитулец Наталья Николаевна – ведущий научный сотрудник, кандидат биологических наук, доцент;
Ничипорук Ольга Ивановна – ведущий специалист;
Якубович-Ботяновская Анна Евгеньевна – ведущий специалист;
Дирко Вадим Николаевич – ведущий специалист;
Борисова Светлана Сергеевна – ведущий специалист;
Кучинская Дарина Викторовна – лаборант 1 категории;
Клемезь Елизавета Геннадьевна – лаборант 1 категории;
Стаховская Маргарита Васильевна – лаборант 1 категории;
Зеневич Мечислава Александровна – лаборант.
Лаборатория контроля качества иимунобиологических лекарственных средств укомплектована современным оборудованием.

|
Анализатор растворения таблеток и капсул |

|
Анализатор растворения суппозиторий SТ-35 |

|
Криоскопический осмометр «OSMOMAT 3000» (посередине), Лабораторный гомогенизатор (справа) |

|
Фотометр флуоресцентный микропланшетный FLUOstar Omega |

|
Хроматограф жидкостной высокоэффективный |

|
Электрофорез капиллярный |
| Микропланшетный промыватель | |

|
Микропланшетный фотометр SPECTROstar Omega |

|
Весы лабораторные электронные |

|
Рабочая станция для калибровки пипет-дозаторов |

|
Система изоэлектрофокусирования с охладителем |

|
Система горизонтального гель-электрофореза |

|
Система очистки воды Arium advance EDI |

|
Автоматический настольный автоклав |

|
Лабораторная печь SLW 180 POL-EKO |

|
Лабораторный морозильник (-40 С) ULUF 120, Холодильник лабораторный MEDICA 250 ECT-F-A 120, Холодильник лабораторный TC 230 |

|
Лабораторный холодильник IRIDIUMNext 520 V-4-STD |

|
Проточный цитометр |

|
Кюветный спектрофотометр EMC-61PCS-UV |

|
Гелевая система для формирования изображений |

|
Анализатор размера частиц Мastersizer 3000 с диспергатором HYDRO EV |

|
Инкубатор BF-260 |
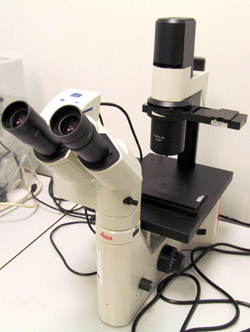
|
Инверсионный микроскоп с камерой |

|
Дозаторы пипеточные |

|
Аварийная душевая Установка и станция для промывки глаз |

|
Бокс перчаточный |

|
Камера эвтаназии СО2 |

|
Биозащитная станция работы с животными |

|
Бокс микробиологической безопасности SafeFAST Elite-S/D |

|
Стеллаж для клеток кроликов в комплекте |

|
Стеллаж для клеток мышей лабораторных в комплекте |

|
Стеллаж для клеток морских свинок в комплекте |
В лаборатории ежегодно выполняются испытания по контролю качества около 1500 серий ИЛС отечественного и зарубежного производства до их реализации, а также находящихся в обращении на территории Республики Беларусь, проводятся адаптация и апробация методов проверки качества ИЛС на стадии их регистрации на территории страны.
Уровень компетентности специалистов подтверждается сертификатами участников межлабораторных сличительных испытаний, проводимых Провайдером проверки квалификации поверочных, калибровочных и испытательных лабораторий, РУП «Белорусский государственный институт метрологии.
Лаборатория аккредитована на соответствие требованиям ГОСТ ISO/IEC 17025-2019 на проведение испытаний лекарственных средств, фармацевтических субстанций по следующим характеристикам (показателям, параметрам):
упаковка;
маркировка;
описание;
прозрачность и степень мутности жидкостей;
степень окрашивания жидкостей;
потенциометрическое определение рН;
электрофорез с натрием додецилсульфатом в полиакриламидном геле (ДСН-ПАГ);
денатурирующий электрофорез в полиакриламидном геле;
зональный электрофорез в агарозном геле;
пирогенность;
аномальная токсичность;
бактериальные эндотоксины;
иммунохимические методы;
высокоэффективная жидкостная хроматография;
осмоляльность;
загрязнение механическими включениями: невидимые частицы;
механические включения: невидимые частицы.
Вне области аккредитации лаборатория проводит испытания по определению размера частиц методом лазерной дифракции, специфической активности на культуре клеток, лабораторных животных биологических лекарственных средств.
Осуществление контроля качества ИЛС обеспечивает насыщение рынка республики качественной фармацевтической продукцией, что повышает уровень биобезопасности страны.
Специалисты лаборатории являются членами Экспертного совета по иммунизации Минздрава, Республиканской формулярной комиссии Минздрава, экспертной комиссии для предоставления заключения о соответствии/несоответствии лекарственных средств требованиям заявки на закупку Минздрава (раздел J06 «Иммунные сыворотки и иммуноглобулины», J07»Вакцины», V01»Аллергены», V04»Диагностические препараты»), комиссии по лекарственным средствам Минздрава.
Специалисты лаборатории принимают активное участие в разработке статей Фармакопеи ЕАЭС, являясь членами Фармакопейного комитета ЕЭК, специализированной экспертной группы по биологическим лекарственным средствам Фармакопейного комитета ЕЭК, а также Рабочей группы по формированию общих подходов к регулированию обращения лекарственных средств в рамках Евразийского экономического союза при коллегии Евразийской экономической комиссии.
Неоднократно специалисты лаборатории участвовали в инспектировании зарубежных производителей лекарственных средств на соответствие их производств требованиям GMP Республики Беларусь с целью регистрации производимой ими продукции на территории страны.
 Правовой форум Беларуси
Правовой форум Беларуси
 Санитарно-эпидемиологическая служба города Минска
Санитарно-эпидемиологическая служба города Минска
 ГУ «Республиканский центр гигиены, эпидемиологии и общественного здоровья»
ГУ «Республиканский центр гигиены, эпидемиологии и общественного здоровья»
 Белорусский государственный медицинский университет
Белорусский государственный медицинский университет
 Министерство здравоохранения Республики Беларусь
Министерство здравоохранения Республики Беларусь
 Президент Республики Беларусь
Президент Республики Беларусь